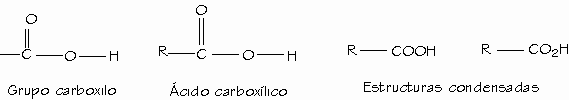PREINFORME 3
Propiedades físicas y químicas de los ácidos carboxilicos
Objetivos:
- Observar las propiedades físicas de los ácidos carboxílicos
- Realizar pruebas de solubilidad y de identificación del grupo carboxílico.
Marco teórico:
Los ácidos carboxílicos son compuestos orgánicos que contienen uno, dos o más grupos carboxilo (—COOH o —CO2H).
El más simple es el ácido metanoico (ácido fórmico), y uno de los más familiares es el ácido etanoico (ácido acético), que en estado diluido e impuro forma parte del vinagre. Los ácidos carboxílicos con un único grupo carboxilo y, generalmente, de cadena lineal se denominan ácidos grasos; la cadena hidrocarbonada puede ser saturada o bien contener uno o más enlaces dobles. Muchos ácidos carboxílicos son esenciales en la química de los organismos vivos. Otros son productos químicos de gran importancia industrial.
Propiedades físicas
Los ácidos de masa molar baja (hasta diez átomos de carbono) son líquidos incoloros, de olor muy desagradable. El olor del vinagre se debe al ácido acético; el de la mantequilla rancia al ácido butírico. El ácido caproico se encuentra en el pelo y secreciones del ganado caprino. Los ácidos C5 a C10 poseen olores a “cabra”. El resto sólidos cerosos e inodoros a temperatura ambiente. Sus puntos de fusión y ebullición crecen al aumentar la masa molar.
Los ácidos inferiores son solubles en agua; su solubilidad decrece a partir del ácido butírico con el aumento del carácter hidrocarbonado de la molécula. Todos los ácidos son solubles en solventes orgánicos
Propiedades químicasAcidez
La reacción más característica de los ácidos carboxílicos es su ionización

Esta ionización se atribuye al desplazamiento electrónico a lo largo del doble enlace del grupo carbonilo hacia el átomo de oxígeno, dejando una carga positiva parcial sobre el átomo de carbono, provocando un desplazamiento inductivo a lo largo de los enlaces C - O y O - H, en sentido opuesto al átomo de hidrógeno, que puede ser extraído por interacción con una base. Por otra parte, el anión producido por la pérdida de un protón es un híbrido de resonancia de dos estructuras canónicas. La deslocalización de la carga estabiliza el anión, por lo que este puede formarse con mayor facilidad Ácidos Carboxílicos
Entre los ácidos alifáticos monocarboxílicos a medida que aumenta el número de carbonos disminuye su acidez porque los grupos hidrocarbonados son donadores de electrones, lo que hace que a mayor número de carbonos se fortalezca el enlace O - H y disminuye la facilidad de la liberación del ión hidrógeno.
Materiales y reactivos:
- gradillas, cinco tubos de ensayo, mechero, mtubo con desprendimiento lateral, pinzas.
- ácido fórmico: corrosivo y venenoso para orgánismos acuaticos.
- ácido acetico: corrosivo e irritante
- ácido oxálico: Irritación y/o corrosión de las mucosas y el esófago.
- ácido estearico: irritante.
- ácido salicílico: irritante
- ácido benzoico: irritante.
- tinta ordinaria
- ácido sulfúrico: corrosivo e irritante.
- KMnO4: Irritante.
- Etanol: en contacto con los ojos es irritante.
- CuSO4: inflamable e irritante.
- NaOH: corrosivo e irritante.
Método experimental: